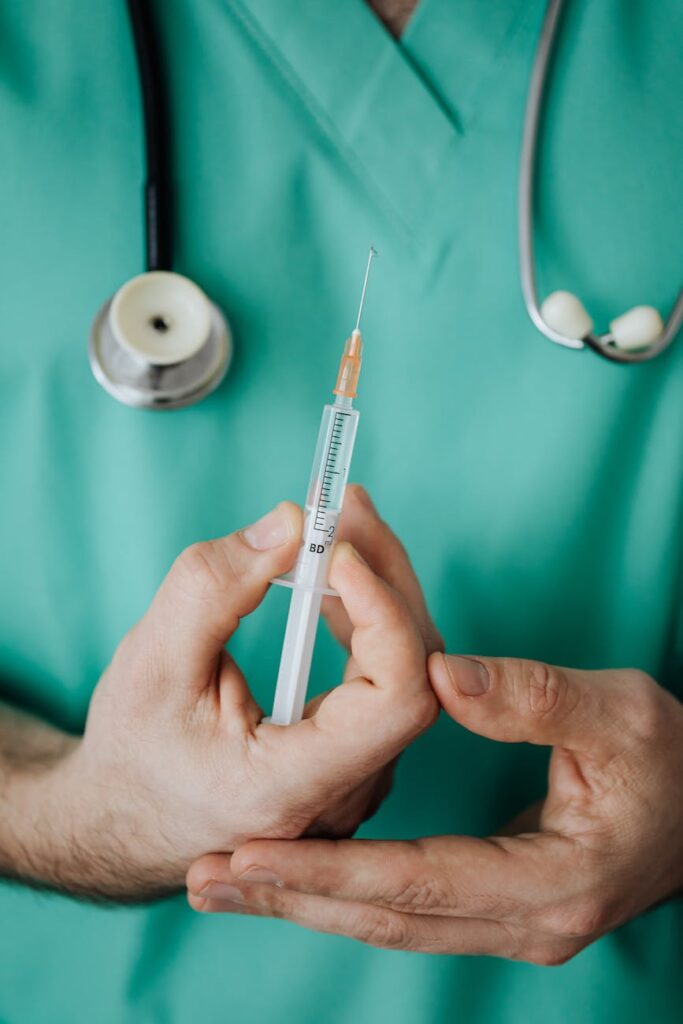
BioVie(NASDAQ:BIVI), 미국간질환연구협회(AASLD)에서 난치성 복수에 대한 BIV201의 2b상 시험에서 긍정적인 임상 안전성 데이터 발표 – The Liver Meeting® 2023
데이터에 따르면 표준 치료(SOC)와 병용한 BIV201은 SOC 단독 요법과 비교하여 치료 후 발생한 부작용(TEAE)에 큰 차이가 없이 내약성이 우수합니다.
난치성 환자의 사망률이 약 50%에 달하는 1 , 2b상 임상시험의 유효성 및 안전성 결과로 BIV201의 확증 임상시험 가속화 지원
회사, 2024년 2분기에 3상 임상시험 시작 약속 재확인
네바다주 카슨시티, 2023년 11월 13일 (GLOBE NEWSWIRE) — BioVie Inc., (NASDAQ: BIVI) (“BioVie” 또는 “회사”)는 진행성 질환 치료를 위한 혁신적인 약물 치료법을 개발하는 임상 단계 회사입니다. 간 질환 및 신경 및 신경퇴행성 질환이 불응성 복수 환자를 대상으로 표준 치료(SOC)와 함께 연속 주입으로 투여되는 테르리프레신 BIV201의 효능과 안전성을 평가하는 회사의 2b상 공개 라벨 연구에서 얻은 긍정적인 임상 안전성 데이터를 오늘 발표했습니다. 간경변으로 인해. 이 데이터는 오늘 The American 에서 “비보상성 간경변증 및 불응성 복수 환자에 대한 연속 주입 테리프레신(BIV201)의 안전성 및 내약성: 2상, 무작위, 대조, 공개 라벨 연구”라는 제목의 최신 포스터 프레젠테이션에서 강조될 예정 입니다 . 간 질환 연구 협회(AASLD) – 매사추세츠주 보스턴에서 열리는 간 회의® 2023 .
“우리의 2b상 결과는 진단 후 1년 이내에 생존율이 50%에 불과한 난치성 복수가 있는 간경변증 환자에게 치료법을 제공하기 위한 중요한 단계입니다. 1 현재 이러한 환자들을 위한 유일한 옵션은 경정맥간내 문맥전신단락술(TIPS) 수술이나 간 이식뿐이며, 이는 침습적이고 삶을 변화시킬 수 있는 수많은 합병증을 수반합니다.”라고 BioVie의 사장 겸 CEO인 Cuong Do가 말했습니다. “제시된 데이터는 통계적으로 유의미한 효능과 결합되어 BioVie가 완료되기 전에 시험을 중단하고 2024년 2분기에 시작될 것으로 예상되는 BIV201의 3상 시험 개발을 가속화하는 데 대한 자신감을 더욱 강화할 수 있었습니다.”
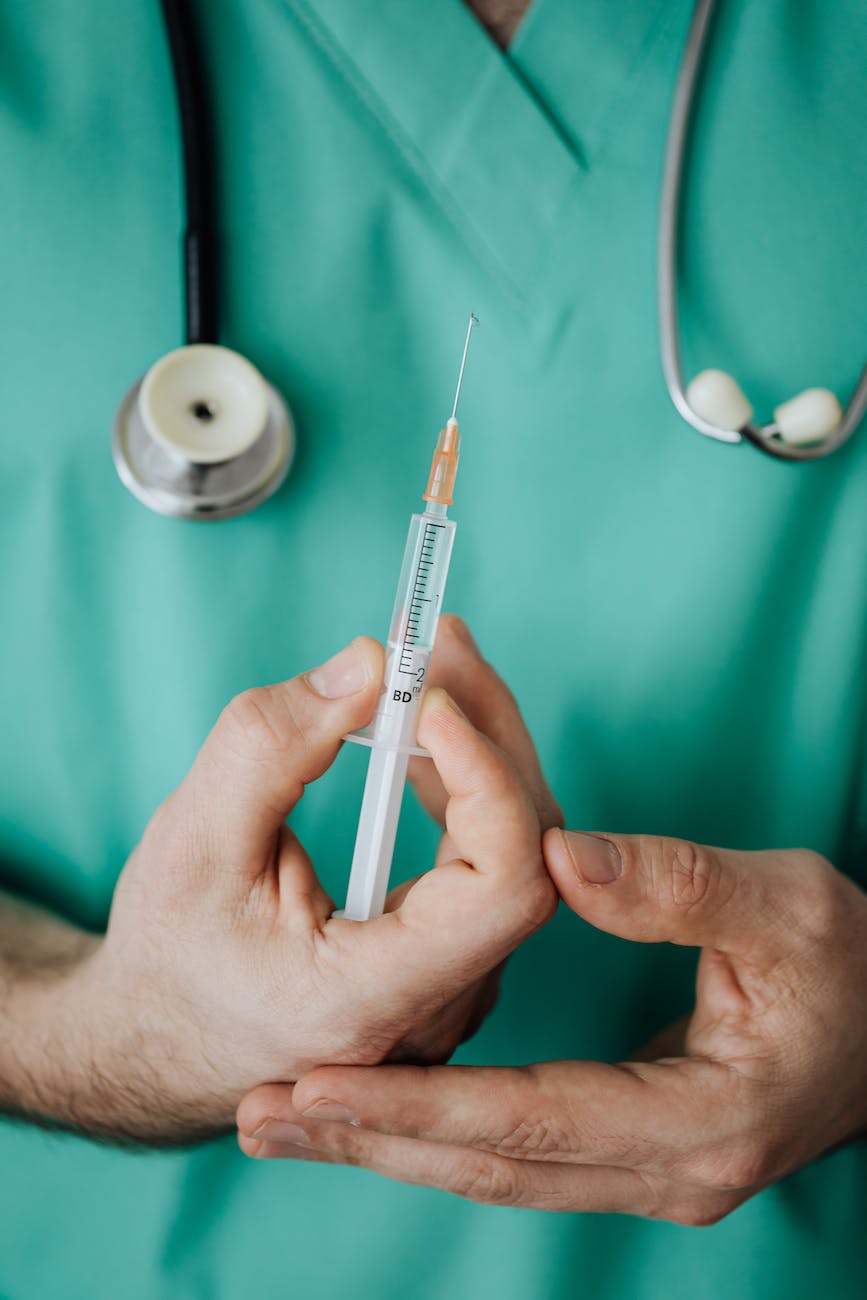
결과는 BIV201과 SOC의 병용요법이 내약성이 우수하고 유리한 안전성 프로파일을 가지고 있음을 보여주었습니다. 심각한 TEAE를 포함한 치료 관련 부작용(TEAE)의 발생률은 두 치료군에서 유사했습니다. BIV201을 투여받은 2명의 환자는 점차적으로 발생하는 저나트륨혈증을 경험했으며, 증상은 없었고, 연구 약물을 중단하면 해결되었습니다. 2a상 연구(환자 6명, 총 BIV201 주입 일수 131일) 및 2b상 연구(환자 10명, BIV201 주입 총 379일)의 누적 안전성 데이터는 관련된 심각한 부작용이 단 1건인 이 모집단의 안전성과 내약성을 더욱 뒷받침합니다. 테리프레신에. 연구자들은 이번 발견이 비대상성 간경변증 환자의 이뇨제 저항성 복수 치료를 위한 확증 시험에서 BIV201의 추가 개발 및 조사를 장려한다고 결론지었습니다.
2b상 시험은 간경변증과 난치성 복수가 있는 성인 환자를 무작위로 28일 2회 치료 기간 동안 SOC와 함께 BIV201을 투여하거나 SOC 단독 투여군으로 무작위 배정한 용량 적정 대조 연구였습니다. 휴약 간격으로 구분된 치료 기간과 180일의 장기 추적 기간이 이어집니다. 1차 종료점은 무작위 배정 후 180일 동안 안전성, 내약성, 특정 합병증(등급 ≥2)의 발생률이었습니다.
복수는 간 및 신장 기능 장애로 인해 복부에 다량의 체액(종종 5리터 초과)이 축적되는 진행성 간경변의 일반적인 합병증입니다. 난치성 복수로 진행된 환자의 1년 생존율은 약 50% 1 입니다 . 현재까지 불응성 복수에 대해 특별히 승인된 의학적 치료법은 없습니다. 이들 환자의 관리는 일시적인 완화만 제공하고 질병 개선 효과가 부족하며 생명을 위협하는 합병증을 빈번하게 초래하는 대용량 복수천자 및 TIPS와 같은 절차를 기반으로 합니다.
테르리프레신 연속주입제인 BIV201은 2017년 미국 식품의약국(FDA)으로부터 복수 치료용 희귀의약품 지정을 받았습니다. 테르리프레신은 현재 40개국 이상에서 간경변 관련 합병증 치료에 사용되고 있지만, 미국이나 미국에서는 사용할 수 없습니다. 일본. BioVie는 2024년 2분기에 시작되는 중요한 3단계 시험을 실시할 계획입니다. 포스터는 오늘 11월 13일 오후 1시부터 오후 2시까지 발표됩니다.
BioVie(NASDAQ:BIVI)주식소개
임상 단계의 바이오제약 회사인 BioVie Inc.는 미국에서 만성 쇠약 상태 치료용 약물의 발견, 개발 및 상업화에 참여하고 있습니다. 제품 파이프라인에는 만성 간경변으로 인한 복수 치료에 대한 임상 2a상 시험을 완료한 BIV201, 및 염증성 세포외 단일 조절 키나제의 잠재적으로 선택적인 억제제인 NE3107은 경도에서 중등도의 알츠하이머병 환자 치료를 위한 임상 3상 시험과 파킨슨병 치료를 위한 임상 2상 시험이 진행 중입니다. 이 회사는 이전에 NanoAntibiotics, Inc.로 알려졌으며 2016년 7월에 BioVie Inc.로 이름을 변경했습니다. BioVie Inc.는 2013년에 법인화되었으며 네바다주 카슨 시티에 본사를 두고 있습니다.
BioVie의 주가전망
2명의 주식 리서치 분석가가 BioVie 주식에 대한 1년 가격 목표를 발표했습니다. BIVI 주가 목표 범위는 $11.00에서 $12.00입니다. 평균적으로 그들은 회사의 주가가 향후 12개월 내에 11.50달러에 도달할 것으로 예상합니다. 이는 현재 주가 대비 265.1%의 상승 여력이 있음을 의미한다.
BioVie의 공매도
BioVie는 10월 한 달 동안 공매도가 증가한 것을 확인했습니다. 10월 31일 현재 공매도량이 총 2,650,000주로 10월 15일 총 2,120,000주보다 25.0% 증가했습니다. 일평균 거래량 337,600주 기준 현재 공매도율은 7.8일이다. 회사 주식의 약 19.9%가 공매도되었습니다.
BioVie의 다음 수익발표 예정일
회사는 2024년 2월 9일 금요일에 다음 분기별 수익 발표를 발표할 예정입니다.